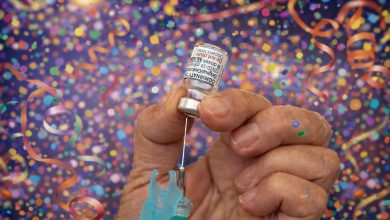
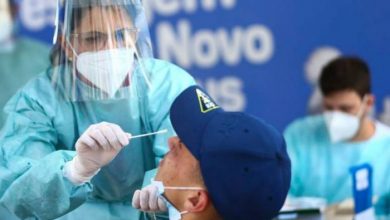
Anvisa autoriza volta dos testes da vacina contra covid-19 do Butantan
A Anvisa (Agência Nacional de Vigilância Sanitária) autorizou nesta quarta-feira (11) a retomada dos testes da vacina contra a covid-19 coordenados pelo Instituto Butantan em parceria com a farmacêutica chinesa Sinovac. A pesquisa foi interrompida na segunda-feira (9), após morte de um voluntário que não tem relação com o imunizante, de acordo com o Butantan e especialistas envolvidos no estudo.
Os integrantes do governo de São Paulo, de João Doria (SP), acusam a agência ligada ao governo de Jair Bolsonaro, opositor político do tucano, de atuar para minar a credibilidade da vacina. A cúpula da agência nega as acusações. Bolsonaro, por outro lado, chegou a comemorar a interrupção dos testes, que atrasa o calendário do Butantan.
Em nota publicada nesta quarta, a Anvisa informou que “acaba de autorizar a retomada do estudo clínico relacionado à vacina Coronavac, que tem como patrocinador o Instituto Butantan”.
“Após avaliar os novos dados apresentados pelo patrocinador depois da suspensão do estudo, a Anvisa entende que tem subsídios suficientes para permitir a retomada da vacinação e segue acompanhando a investigação do desfecho do caso para que seja definida a possível relação de causalidade entre o evento adverso grave inesperado e a vacina”, diz o texto.
Apesar de eventos desse tipo serem comuns em testes de vacinas, a forma como a agência atuou foi criticada por cientistas e por sanitaristas. Após a decisão, tanto a Anvisa quanto o Butantan divulgaram versões conflitantes sobre o que ocorreu.
Os testes da Coronavac são coordenados pelo Butantan, mas feitos em centros participantes em diversas cidades, como São Paulo, Brasília, Belo Horizonte e Rio de Janeiro, por exemplo. O óbito foi de um voluntário monitorado pelo Hospital das Clínicas, ligado à USP (Universidade de São Paulo).
De acordo com um comunicado infectologista Esper Kallas, responsável pelos voluntários no HC, “a equipe de investigadores fez uma análise criteriosa sob o ocorrido e concluiu que o evento não está relacionado à vacina em teste”. O médico também afirmou que o caso foi comunicado à Anvisa e à Conep (Comissão Nacional de Ética em Pesquisa), mas não cita qualquer comunicação ao comitê internacional independente.
Essa supervisão externa é uma exigência para realizar testes clínicos e tem como objetivo garantir o cumprimento de prazos previstos pelos pesquisadores e que decisões tomadas não coloquem em risco a segurança dos participantes ou integridade do estudo. Esse colegiado é formado por chefes independentes e pode ter representantes dos centros participantes.
Ao explicar o motivo da suspensão, a Anvisa alegou que só poderia autorizar a retomada dos testes após o comitê assegurar que o óbito não tinha relação com o imunizante. O colegiado fez essa recomendação na terça, após a controvérsia sobre a pausa nos testes se instalar.
O presidente da Anvisa afirmou que “só um grupo muito restrito de pessoas sabe se o voluntário tomou placebo ou não” e que essa informação viria do comitê independente. Os testes clínicos são feitos de forma que quem recebe e quem aplica as doses não sabe se o voluntário recebeu o placebo ou o imunizante, o que é chamado de “duplo cego”.
Essa informação é “quebrada” para os pesquisadores nos casos de eventos adversos. Quando não é o caso de morte, o voluntário deixa o estudo para preservar a integridade da pesquisa, já que a informação sobre o grupo a que pertence deixa de ser sigilosa.
O que houve com o voluntário?
O Instituto Butantan informou que o participante recebeu a dose da vacina ou do placebo ”nos primeiros dias do mês de outubro” e que “após 25 dias [da aplicação], aproximadamente, ele foi encontrado sem vida”.O Hospital das Clínicas foi notificado no dia seguinte, quando iniciou a apuração do caso, de acordo com nota enviada ao HuffPost Brasil.
Nenhum integrante do governo de São Paulo ou do governo federal confirmou a informação divulgada pela imprensa de que o óbito teria sido um suicídio.
De acordo com o pesquisador da Universidade Federal do Rio de Janeiro (UFRJ) e infectologista Mauro Schechter, não seria possível relação entre esse tipo de morte e a vacina devido ao intervalo de tempo. ”Se o suicídio ocorresse nas horas seguintes [à aplicação da dose] ou se esse paciente tivesse um relato de alteração de comportamento nas horas seguintes, você poderia dizer que ele teve uma encefalite pela vacina”, exemplificou.
Para o cientista, os procedimentos feitos pelos pesquisadores ligados ao governo de São Paulo bastariam para que os testes não fossem interrompidos e não é comum agências reguladoras tomarem esse tipo de decisão. “Isso é uma decisão política ou completo desconhecimento por parte do presidente da Anvisa de como funcionam estudos clínicos”, afirmou ao HuffPost Brasil o professor associado da Johns Hopkins University.
Por outro lado, em caráter reservado, cientistas e sanitaristas que fizeram parte da cúpula da Anvisa criticaram o fato de a composição do comitê independente nunca ter sido divulgada e lamentaram a atuação de ambos os lados. Uma das fontes ouvidas, afirmou que “o comitê é importante, mas a palavra final é da Anvisa, e nesse clima criado pelo presidente, governador e Butantan, todos estão perdendo a razão”.
De acordo com o Butantan, em 30 de outubro, o HC informou a Conep “e a Farmacovigilância do Instituto Butantan (patrocinador do estudo)”, sobre o evento adverso. “No dia 6 de novembro, dentro do prazo, a farmacovigilância do Instituto Butantan comunica a Agência Nacional de Vigilância Sanitária (Anvisa), conforme preconizado em protocolo oficial. Na conclusão constava que o óbito não era relacionado à vacina em teste”, também de acordo com a nota do instituto de pesquisa.
A equipe da Anvisa alega que o comunicado enviado no dia 6 não chegou à agência por problemas técnicos de hackeamento. O gerente-geral de Medicamentos da agência, Gustavo Mendes, atribuiu a falha ao ataque cibernético sofrido pelo governo federal na última semana. Segundo Mendes, a informação chegou na segunda-feira (9), quando a Anvisa anunciou a suspensão dos testes.
O presidente da Anvisa, Antonio Barra Torres, também disse que as informações fornecidas inicialmente eram “incompletas e insuficientes”. “Documentos claros, precisos e completos têm de ser enviados a nós, o que não aconteceu”, disse em coletiva de imprensa no início da tarde desta terça.
De acordo com o Butantan, em 6 de novembro, o instituto “recebeu um ofício às 15h por meio de caixa postal, ferramenta mantida dentro do sistema da Anvisa, solicitando informações sobre eventos adversos graves inesperados entre os dias 30 de outubro até 9 de novembro”.
Também na segunda, o instituto recebeu um e-mail da agência com o mesmo conteúdo às 18h13, que foi respondido pelo Butantan às 18h24, com cópia “das notificações ocorridas no período solicitado e que já haviam sido encaminhadas via sistema à Anvisa no dia 6 de novembro”.
No mesmo dia, às 20h47, o Butantan recebeu convite por e-mail para uma reunião emergencial na manhã desta terça, sem o assunto especificado. ”Às 21h04, um novo ofício foi depositado pela Anvisa na caixa postal do sistema, informando sobre a suspensão do estudo”, segundo o Butantan. Em seguida, a Anvisa comunicou a imprensa sobre a interrupção dos estudos clínicos.
Na nota publica nesta quarta, a Anvisa diz que não conhecia a causa do evento adverso grave, que só teria sido informada pelo Butantan na manhã de quarta, quando decidiu pela interrupção. Também segundo a agência, só na tarde de ontem foi enviado o boletim de ocorrência sobre o óbito e à noite chegou a avaliação do comitê.
“A medida, de caráter exclusivamente técnico, levou em consideração os dados que eram de conhecimento da Agência até aquele momento e os preceitos científicos e legais que devem nortear as nossas ações, especialmente o princípio da precaução que prevê a prudência, a cautela decisória quando conhecimento científico não é capaz de afastar a possibilidade de dano”, diz o texto.
Nesta quarta, a agência informou que esse tipo de interrupção é comum e “não significa necessariamente que o produto sob investigação não tenha qualidade, segurança ou eficácia”.
A decisão da Anvisa pode prejudicar o acesso à vacina?
O Instituto Butantan fará uma análise preliminar dos resultados de eficácia da candidata à vacina quando forem atingidos 61 casos confirmados de covid-19 entre os voluntários. Se houve 50% de imunizados neste grupo, esses dados podem permitir um registro emergencial para liberar a aplicação das doses, após aval da Anvisa.
Se esse percentual não for atingido, o ensaio clínico segue até alcançar 150 casos, quando será analisada a eficácia nessa amostra maior.
Embora a previsão seja de que 13 mil pessoas participem do estudo – e ao menos 9 mil já receberam o imunizante ou o placebo –, os 61 casos ainda não foram atingidos. Um dos possíveis motivos é a queda na circulação do vírus no Brasil, já que, para alcançar os resultados, é necessário que os voluntários entrem em contato com o SARS-CoV-2.
O presidente do Instituto Butantan, Dimas Covas, afirmou que a forma como a Anvisa atuou pode reduzir a adesão dos voluntários, o que atrasaria os resultados. “Suspender um estudo clínico, causar incerteza, causar medo nas pessoas, fomentar um ambiente já não muito próprio ao fato de essa vacina ser feita em associação com a China. Fomentar esse descrédito gratuito a troco de que?”, questionou.
A decisão foi tomada no dia em que Doria anunciou a chegada de 120 mil doses da Coronavac em 20 de novembro. O estoque ficará guardado até o produto receber o registro da Anvisa, o que só poderá ocorrer após a eficácia ser comprovada.
Quais vacinas poderão chegar até os brasileiros?
Essa é uma das 3 possibilidades de os brasileiros terem acesso a uma vacina contra a covid-19. Embora os testes da Coronavac estejam avançados, há dúvidas de como ela seria distribuída, caso seja comprovada sua eficácia. Em geral, cabe ao Ministério da Saúde, por meio do Programa Nacional de Imunização (PNI), definir a estratégia de vacinação, o que inclui decisões sobre grupos prioritários, número de doses e o calendário de distribuição em todos os estados, em coordenação com as secretarias estaduais de Saúde.
Mas essa incorporação ainda não foi feita pelo governo federal, em meio à briga entre Bolsonaro e Doria. Até agora, o ministério trabalha com outras duas frentes. O acordo com a farmacêutica britânica AstraZeneca, responsável pelo produto desenvolvido pela Universidade de Oxford, prevê acesso a 100,4 milhões de doses para o primeiro semestre e insumos que permitirão a produção de outras 110 milhões de doses no segundo semestre de 2021, pelo Bio-Manguinhos, laboratório da Fiocruz.
Já a Covax-Facility garantiria outras 42 milhões de doses. A iniciativa global funciona como uma coalizão em que os países participantes dividem o risco de investimento tecnológico e apostam em várias iniciativas de imunizantes. Em troca, podem ter acesso à vacina que se provar segura e eficaz. Entre as candidatas do grupo, está a desenvolvida pela Universidade de Oxford e outros 8 imunizantes.